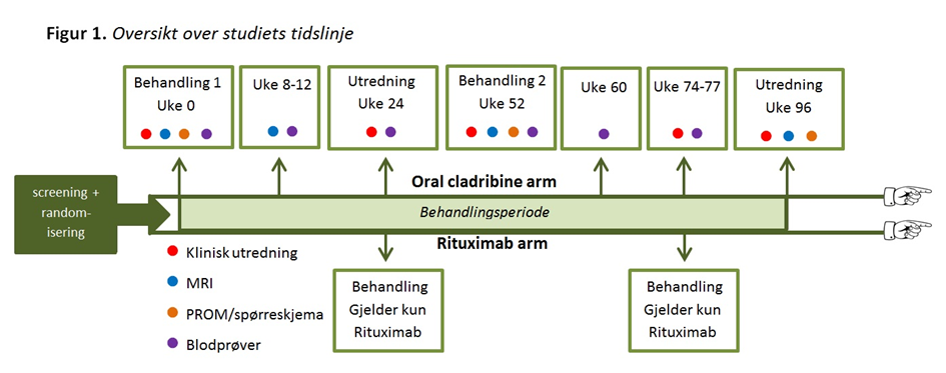
Norsk studie av kladribin og rituksimab ved Multippel Sklerose (NOR-MS).
En prospektiv åpen multisenter-studie med blindet endepunkt.
Formålet med studien er å finne ut om rituksimab er like effektivt, trygt og brukervennlig som kladribin. Rituksimab er ikke en godkjent på vanlig måte som MS-medisin, men det er mange studier som tyder på at den er like effektiv, trygg og brukervennlig som andre høyeffektive behandlinger mot MS, og medikamentet brukes mot MS også i Norge. Denne studien vil gi oss svar på om behandling med rituksimab er likeverdig med behandling med kladribin.
Rituksimab og kladribin virker på litt forskjellig måte. Rituksimab gis som infusjon hvert halvår og fører til at en undergruppe immunceller i blodet (CD20-positive B-celler) blir sterkt redusert over tid. Dette demper MS-aktiviteten drastisk.
Kladribin gis som to korte tablettkurer (i uke 0 og uke 4 ved starten av behandlingen) og dette gjentas etter ett år. Behandlingen fører til at flere typer immunceller (B-celler og noen T-celler) i kroppen blir midlertidig redusert, og at de senere delvis endrer virkemåte. Denne behandlingen fører også til at MS-aktiviteten dempes drastisk. Etter gjennomført behandling vil man vanligvis oppnå en langvarig beskyttelse mot aktivitet i MS-sykdommen.
Det er aldri gjort noen studier tidligere for å sammenligne disse to typene MS-behandlinger direkte. Denne studien er derfor viktig for å finne ut hvordan vi bør behandle MS-pasienter best mulig i fremtiden.
I tillegg til å se på effekt, sikkerhet og pasienttilfredshet, skal vi undersøke om det er bestemte markører, enten fra MR-bilder eller fra blodprøver, som kan bidra til å forutse hvilken medisin som vil være best egnet hos den enkelte pasient. Vi vil også undersøke de helseøkonomiske konsekvensene av å tilby de forskjellige medikamentene.
Man kan delta i studien dersom man er mellom 18 og 65 år og har attakkvis MS med tegn på sykdomsaktivitet det siste året (MR-forandringer eller et nytt attakk) og legen din mener man vil ha utbytte av høyaktiv behandling med rituksimab eller kladribin. Man kan med disse behandlingene ikke planlegge å bli gravid de neste to årene og må bruke prevensjon dersom du er kvinne i fertil alder. Man kan ikke ha noen kjent kreftsykdom eller ha fått behandling med medikamentene rituksimab, kladribin, alemtuzumab eller ha fått stamcellebehandling tidligere. Man må heller ikke ha blitt behandlet med fingolimod eller natalizumab de siste 6 månedene. Alle pasienter ved sykehuset der man behandles, som oppfyller kriteriene over, kan bli forespurt om å delta.
Nevrologisk avdeling ved Oslo Universitetssykehus er ansvarlig for studien. Den daglige oppfølgingen av pasientene i studien vil foregå av legen som behandler deg på det sykehuset der man hører til.